Ученые и журналисты: США заранее готовились к COVID-19
Школа Души Божественного Космоса :: В поисках правды: инсайдеры и теории заговоров :: Разоблачители коронамракобесия
Страница 1 из 1
 Ученые и журналисты: США заранее готовились к COVID-19
Ученые и журналисты: США заранее готовились к COVID-19
Ученые и журналисты: США заранее готовились к COVID-19
https://www.pravda.ru/world/1482450-COVID19/
https://www.pravda.ru/world/1482450-COVID19/
- 1:
Ученые и журналисты: США заранее готовились к COVID-19
Мир
Китай вытащил на свет божий исследовательскую работу 2015 года о том, что коронавирус был создан учеными в сотрудничестве с американской армией.
Такой материал появился в 2015 году на сайте научного журнала Natura в 2015 году. Тогда авторы утверждали, что после появления вируса атипичной пневмонии (2002-2003) и Ближневосточного респираторного синдрома (MERS) ученые знали о риске межвидовой передачи, которая приведет к эпидемии среди людей.Успешный лабораторный эксперимент
В числе прочего исследовательская группа изучала летучих мышей, которые являются крупнейшими инкубаторами коронавирусов. Тем не менее летучие мыши не могли передавать людям коронавирус, потому что они не могли взаимодействовать с клетками человека с АСЕ2-рецепторами.
Чтобы лучше изучить данный вирус, ученые скопировали коронавирус и инфицировали им лабораторных мышей. Результаты показали, что вирус действительно способен связываться с клетками человека с АСЕ2-рецепторами и размножаться в клетках дыхательной системы.В материале также говорилось, что подковоносные летучие мыши несут штамм коронавируса SARS, который способен передаваться людям. Он был назван вирусом SHC014-CoV.
В исследовательской работе отмечается, что лабораторные материалы, образцы и оборудование, которые использовались при проведении исследований, были получены из Армейского медицинского научно-исследовательского института инфекционных заболеваний. Хотя пока невозможно утверждать наверняка, что вирус, который был испытан на лабораторных мышах, тот же самый, что и коронавирус SARS-Cove-2.Политика НАТО
Впрочем, интересные вещи можно найти и в более ранних документах. К примеру:- В отчете о деятельности альянса НАТО за 2019 год говорится, что в 2019 году первое место в научно-исследовательской работе альянса заняла тема радиохимической и биологической защиты (29%), сместив казалось бы самую насущную проблему Европы — противодействие терроризму (оно оказалось на 4-м месте по приоритетности).
- Годом ранее, в 2018, ситуация была прямо противоположная: терроризм, как и должно быть, был на первом месте (28%), а радиохимическая и биологическая защита на четвертом (13%).
Как пишут в телеграм-канале "Брюссельский стукач", "учитывая отсутствие видимых причин столь резкой смены научных интересов, варианта два и оба они нелицеприятные:- либо НАТО сейчас виляет пятой точкой, фальсифицируя данные, чтобы показать "а мы к вирусам всегда готовились, мы же современные",
- либо еще в 2019 году в альянсе, прости Господи, знали откуда придет беда.
[size]
Да, первый вариант куда более реален, но, согласитесь, факты удивляют".[/size]Отношения с Россией
Там же можно сравнить и риторику по поводу отношений с Россией.
Последний отчет гласит, что "все более-менее, работаем. И только последний абзац параграфа про обеспокоенность "поведением Москвы в Европе".
В докладе за 2018 г. ситуация, опять же, была диаметрально противоположной. 90% параграфа Россию обвиняли в смертных грехах и как бы между строк упоминали про сотрудничество.Символическое смягчение риторики НАТО в адрес России, полагаю, вызвано нежеланием многих европейских стран альянса, чьи представители участвовали в подготовке документа, обострять отношения с Москвой. Особенно на фоне всего, что происходит сейчас в Европе и мире. То есть, когда нужно — про "несусветное русское зло" готовы на время подзабыть".Военные расходы США
При этом в 2019 году доля военных расходов США в совокупном военном бюджете стран НАТО составляла 70%, европейских членов с Канадой — 30%.
В 2018 году те же самые показатели были на уровне 69,3% и 30,7% соответственно. Количество стран, выполняющих рекомендации НАТО по закупке военной техники (20% от военного бюджета страны), осталось прежним.
Но в прошлом году НАТО получил 8,5 млн. евро на закупку серверов баз данных согласно решения о разработке "Системы ПВО наземного базирования 21-го века" (21st CenturyGround Based Air Defence). Последнее означает, что НАТО продолжает активную работу по улучшению (как по качеству, так и по скорости) возможностей обмена разведывательными данными между всеми странами-членами. Вопрос о том, для чего это нужно, можно даже не задавать.Штабные "учения" 2017 года
Напомним, в свое время в 2017 году за неделю до инаугурации Трампа администрация Обамы и новая команда приняли участие в штабной игре по сценариям крупного внутреннего инцидента на территории США.
По информации издания Politico, замысел учений подразумевал реагирование на быстрое развитие смертельной пандемии вируса H9N2, который бушевал в Азии и Англии. В реальности подобной угрозы не существовало на тот момент и ситуация с эпидемией была лишь сценарием для обязательных "учений" переходного периода.
В качестве других вводных рассматривались опустошительный ураган, и кибер-инцидент.
Цель "игры" — предоставить новой администрации понимание методов координации своих усилий в борьбе с угрозами."Сценарий пандемии предусматривал все сопутствующие негативные факторы, которые сейчас наблюдаются в связи с распространением #COVID19
Методы борьбы с пандемией, озвученные в ходе этих брифингов, подразумевали координацию всех институтов власти, скорость принятия решений, научный подход и т. д.
30 сотрудников администрации Трампа приняли участие в этих "учениях", однако большинство из них уже не работают в Белом доме, поэтому, подводят авторы статьи итог, говоря о неожиданном развитии событий с коронавирусом, Трамп мог говорить правду, т. к за прошедшие годы была утеряна преемственность государственного подхода", — пояснили в телеграм-канале "Военный обозреватель".
Читайте больше на https://www.pravda.ru/world/1482450-COVID19/- В отчете о деятельности альянса НАТО за 2019 год говорится, что в 2019 году первое место в научно-исследовательской работе альянса заняла тема радиохимической и биологической защиты (29%), сместив казалось бы самую насущную проблему Европы — противодействие терроризму (оно оказалось на 4-м месте по приоритетности).
dimslav- Сообщения : 15403
Дата регистрации : 2017-04-29
Возраст : 55
 Re: Ученые и журналисты: США заранее готовились к COVID-19
Re: Ученые и журналисты: США заранее готовились к COVID-19
Оригинальное исследование 2015 года Неотредактированное и полное
Кластер циркулирующих коронавирусов летучих мышей, напоминающий атипичную пневмонию, показывает потенциал для появления человекаhttps://www.veteranstoday.com/2021/06/20/pravda-us-army-created-covid-19-in-2015-research-proofs-or-debunking-you-pick/
- 2а:
Опубликовано: 09 ноября 2015
Винеет Д Menachery путем, Бойд л Янт младший, Кари Debbink, Судхакар Agnihothram, Лиза электронная Gralinski, Джессика в Планте, Рейчел L Грэм, Тревор Скоби, Син-Йи Ге, Эрик Ф Дональдсон, ч Скотт Рэнделл, Антонио Lanzavecchia, Уэйн в Мараски, Zhengli-Ли Ши, Ральфа Барич
Nature Medicine том 21, страницы 1508-1513 (2015)
Исправление к этой статье было опубликовано 06 апреля 2016 года
Эта статья была обновленаВведение
Появление коронавирусов тяжелого острого респираторного синдрома (SARS-CoV) и ближневосточного респираторного синдрома (MERS-CoV) подчеркивает угрозу межвидовой передачи инфекции, приводящей к вспышкам среди людей. Здесь мы исследуем болезнетворный потенциал вируса, подобного атипичной пневмонии, SHC014-CoV, который в настоящее время циркулирует в популяциях китайских подковообразных летучихмышей. Используя систему обратной генетики SARS-CoV, мы создали и охарактеризовали химерный вирус, экспрессирующий спайк коронавируса летучих мышей SHC014 в адаптированном к мышам основе SARS-CoV.
Полученные результаты свидетельствуют о том, что вирусы группы 2b, кодирующие спайк SHC014 в основе природной разновидности, могут эффективно использовать множественные ортологи рецептора SARS человеческого ангиотензинпревращающего фермента II (ACE2), эффективно реплицироваться в первичных клетках дыхательных путей человека и достигать титров in vitro, эквивалентных эпидемическим штаммам SARS-CoV. Кроме того, эксперименты in vivo демонстрируют репликацию химерного вируса в легких мышей с заметным патогенезом.
Оценка имеющихся иммунотерапевтических и профилактических методов лечения АТИПИЧНОЙ пневмонии выявила низкую эффективность; - как моноклональные антитела, так и вакцинный подход не смогли нейтрализовать и защитить от заражения CoV с использованием нового спайкового белка.
На основе этих результатов мы синтетически воссоздали инфекционный полноразмерный рекомбинантный вирус SHC014 и продемонстрировали надежную вирусную репликацию как in vitro, так и in vivo. Наша работа предполагает потенциальный риск повторного появления SARS-CoV из-за вирусов, циркулирующих в настоящее время в популяциях летучих мышей.Главная часть
Появление SARS-CoV ознаменовало новую эру в межвидовой передаче тяжелых респираторных заболеваний с глобализацией, ведущей к быстрому распространению по всему миру и массовым экономическим последствиям. С тех пор несколько штаммов, включая штаммы гриппа A H5N1, H1N1 и H7N9, а также MERS-CoV, появились из популяций животных, вызывая значительные заболевания, смертность и экономические трудности для пострадавших регионов. Хотя меры общественного здравоохранения смогли остановить вспышку SARS-CoV, недавние метагеномные исследования выявили последовательности тесно связанных с SARS-подобными вирусами, циркулирующими в популяциях китайских летучих мышей, которые могут представлять будущую угрозу.
Однако одни только данные о последовательностях дают минимальную информацию для идентификации и подготовки к будущим предпандемическим вирусам. Поэтому, чтобы изучить потенциал возникновения (то есть потенциал заражения людей) циркулирующих КОВИДов летучих мышей, мы построили химерный вирус, кодирующий новый зоонозный спайковый белок CoV —из последовательности RsSHC014-CoV, которая была выделена из китайских подковообразных летучих мышей в контексте адаптированного к мыши основы SARS-CoV. Гибридный вирус позволил нам оценить способность нового спайкового белка вызывать болезнь независимо от других необходимых адаптивных мутаций в его естественной основе.
Используя этот подход, мы охарактеризовали CoV-инфекцию, опосредованную спайковым белком SHC014 в первичных клетках дыхательных путей человека и in vivo и проверили эффективность доступных иммунотерапевтических средств против SHC014-CoV. Вместе эта стратегия транслирует данные метагеномики, чтобы помочь предсказать и подготовиться к появлению новых вирусов в будущем.
Последовательности SHC014 и родственного RsWIV1-CoV показывают, что эти CoV являются ближайшими родственниками эпидемических штаммов SARS-CoV (рис. 1а, б); однако существуют важные различия в 14 остатках, связывающих человеческий ACE2, рецептор для SARS-CoV, включая пять, которые являются критическими для диапазона хозяина: Y442, L472, N479, T487 и Y491 (см.
В WIV1 три из этих остатков отличаются от эпидемического штамма SARS-CoV Urbani, но не ожидалось, что они изменят связывание с ACE2 (Дополнительные рис. 1а,б и Дополнительная таблица 1). Этот факт подтверждается обоими экспериментами по псевдотипированию, которые измеряли способность лентивирусов, кодирующих спайковые белки WIV1, проникать в клетки, экспрессирующие человеческий ACE2 (Дополнительный рис. 1) и in vitro анализы репликации WIV1-CoV (ссылка 1). Напротив, 7 из 14 остатков ACE2- взаимодействия в SHC014 отличаются от таковых в SARS-CoV, включая все пять остатков, критичных для диапазона хоста (Дополнительный рис. 1c и Дополнительная таблица 1).
Эти изменения в сочетании с неспособностью псевдотипированных лентивирусов, экспрессирующих спайк SHC014, проникать в клетки (дополнительный рис. 1d), предполагали, что спайк SHC014 не способен связывать человеческий ACE2. Однако аналогичные изменения в родственных штаммах SARS-CoV, как сообщалось , позволяют связывание с ACE2 , что предполагает необходимость дополнительного функционального тестирования для верификации.
Поэтому мы синтезировали спайк SHC014 в контексте репликационно-компетентной, адаптированной к мышам основы SARS-CoV (далее мы будем называть химерный CoV SHC014-MA15), чтобы максимизировать возможности для изучения патогенеза и вакцин у мышей (Дополнительный рис. 2а). Несмотря на предсказания как структурного моделирования, так и экспериментов по псевдотипированию, SHC014-MA15 был жизнеспособен и реплицировался до высоких титров в клетках Vero (дополнительный рис. 2б). Подобно SARS, SHC014-MA15 также требовал функциональной молекулы ACE2 для входа и мог использовать ортологи ACE2 человека, циветты и летучей мыши (дополнительный рис. 2с,г).
Чтобы проверить способность спайка SHC014 к опосредованному заражению дыхательных путей человека, мы исследовали чувствительность эпителиальной линии клеток дыхательных путей человека Calu-3 2B4 (ref. 9) к инфекции и обнаружили устойчивую репликацию SHC014-MA15, сравнимую с таковой у SARS-CoV Urbani (рис. 1с).
Чтобы расширить эти данные, первичные культуры эпителия дыхательных путей человека (HAE) были инфицированы и показали устойчивую репликацию обоих вирусов (рис. 1d). Вместе эти данные подтверждают способность вирусов с помощью спайка SHC014 заражать клетки дыхательных путей человека и подчеркивают потенциальную угрозу межвидовой передачи SHC014-CoV.
Рис. 1: Вирусы, подобные SARS, реплицируются в клетках дыхательных путей человека и вызывают патогенез in vivo.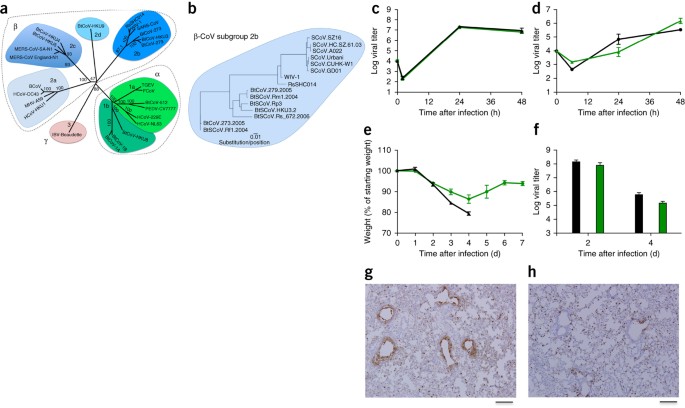
(a) Полнометражные последовательности генома репрезентативных КОВИДов были выровнены и филогенетически картированы, как описано в онлайн-методах. Шкала представляет собой нуклеотидные замены, причем маркируется только поддержка bootstrap выше 70%. Дерево показывает CoV, разделенные на три различные филогенетические группы, определенные как α-CoV, β-CoVи γ-CoV. Классические кластеры подгрупп обозначены как 2a, 2b, 2c и 2d для β-CoVи как 1a и 1b для α-ков. (b) Аминокислотные последовательности доменов S1 спайков репрезентативных β-CoV группы 2b, включая SARS-CoV, были выровнены и филогенетически картированы. Шкала представляет аминокислотные замены. (c,d) Вирусная репликация SARS-CoV Urbani (черный) и SHC014-MA15 (зеленый) после заражения клеток Calu-3 2B4 (c) или хорошо дифференцированных, первичных воздушно-жидких межклеточных культур HAE (d) при кратности заражения (MOI) 0,01 для обоих типов клеток. Образцы собирали в отдельные моменты времени с биологическими копиями (n = 3) как для экспериментов Calu-3, так и для экспериментов HAE. (e,f) Потеря веса (н = 9 для SARS-коронавирус МА15; н = 16 для SHC014-МА15) (е) и вирусной репликации в легких (П = 3 для SARS-коронавирус МА15; П = 4 для SHC014-МА15) (Ф) в 10-недельных мышей линии balb/с, инфицированных 1 × 104 С. Ф.ЕД. мыши-приспособились торс-ков МА15 (черный) или SHC014-МА15 (зеленый) через интраназальный (я.Н.) маршрут. (g,h) Показаны репрезентативные изображения срезов легких, окрашенных на антиген SARS-CoV N от мышей, инфицированных SARS-CoV MA15 (n = 3 мыши) (g) или SHC014-MA15 (n = 4 мыши) (h). Для каждого графика центральное значение представляет среднее групповое значение, а столбики ошибок определяют шкалу s.e.m. (1 мм).
Чтобы оценить роль спайка SHC014 в опосредовании инфекции in vivo, мы заразили 10-недельных мышей BALB/c 104 бляшкообразующими единицами (p.f.u.) либо SARS-MA15, либо SHC014-MA15 (рис. 1e–h). Животные, инфицированные SARS-MA15, испытывали быструю потерю веса и летальность на 4-й день после заражения (d.p.i.); Напротив, инфекция SHC014-MA15 приводила к существенной потере веса (10%), но не летальности у мышей (рис. 1e). Исследование вирусной репликации выявило почти эквивалентные вирусные титры в легких мышей, инфицированных SARS-MA15 или SHC014-MA15 (рис. 1f). В то время как легкие мышей, инфицированных SARS-MA15, показали устойчивое окрашивание как в терминальных бронхиолах, так и в паренхиме легких 2 d.p.i. (рис. 1г), у мышей, инфицированных SHC014-MA15, наблюдалось снижение окрашивания антигенов дыхательных путей (рис. 1н); напротив, не наблюдалось дефицита окрашивания антигенов в паренхиме или в общей гистологической картине, что свидетельствует о дифференциальной инфекции легочной ткани для SHC014–MA15 (дополнительная таблица 2).
Затем мы проанализировали инфекцию у более восприимчивых животных в возрасте 12 месяцев. Зараженные SARS-MA15 животные быстро теряли вес и поддавались инфекции (дополнительный рис. 3а,б). Инфекция SHC014-MA15 вызывала стойкую и устойчивую потерю веса, но имела минимальную летальность. Тенденции в гистологии и паттернах окрашивания антигенами, которые мы наблюдали у молодых мышей, сохранялись и у более старых животных (Дополнительная таблица 3). Мы исключили возможность того, что SHC014-MA15 опосредованно заражал через альтернативный рецептор на основе экспериментов с использованием Ace2 мыш, у которых не наблюдалось потери веса или окрашивания антигеном после заражения SHC014-MA15 (Дополнительный рис. 4а,б и Дополнительная таблица 2). Вместе эти данные указывают на то, что вирусы с шипом SHC014 способны индуцировать потерю веса у мышей в контексте вирулентной основы КоВида.
Учитывая доклиническую эффективность терапии моноклональными антителами к Эболе, такими как ZMapp, мы затем попытались определить эффективность моноклональных антител к SARS-CoV против инфекции SHC014-MA15. Ранее сообщалось о четырех широко нейтрализующих человеческих моноклональных антителах, нацеленных на спайковый белок SARS-CoV, которые являются вероятными реагентами для иммунотерапии. Мы исследовали влияние этих антител на репликацию вируса (выраженное в процентах ингибирования репликации вируса) и обнаружили, что в то время как SARS-CoV Urbani дикого типа был сильно нейтрализован всеми четырьмя антителами при относительно низких концентрациях антител (рис . 2а-d), нейтрализация варьировалась для SHC014–MA15. Fm6, антитело, генерируемое фаговым дисплеем и escape-мутантами, достигало только фоновых уровней ингибирования репликации SHC014-MA15 (рис. 2а). Аналогично, антитела 230.15 и 227.14, которые были получены из В-клеток памяти инфицированных SARS–CoV пациентов, также не удалось заблокировать репликацию SHC014-MA15 (рис. 2b,c). Для всех трех антител различия между спайковыми аминокислотными последовательностями SARS и SHC014 соответствовали прямым или смежным изменениям остатка, обнаруженным у мутантов побега SARS-CoV (fm6 N479R; 230.15 L443V; 227.14 K390Q/E), что, вероятно, объясняет отсутствие нейтрализующей активности антител против SHC014. Наконец, моноклональное антитело 109.8 смогло добиться 50% нейтрализации SHC014-MA15, но только при высоких концентрациях (10 мкг/мл) (рис. 2д). Вместе взятые результаты показывают, что широко нейтрализующие антитела против SARS-CoV могут иметь лишь незначительную эффективность против появляющихся SARS-подобных штаммов CoV, таких как SHC014.
Рис. 2: Моноклональные антитела к SARS-CoV обладают предельной эффективностью против SARS-подобных КОВ.
(a–d)
Анализы нейтрализации оценивают эффективность (измеряемую как уменьшение количества бляшек) панели моноклональных антител, которые все первоначально были сгенерированы против эпидемического SARS-CoV, против заражения клеток Vero SARS-CoV Urbani (черный) или SHC014-MA15 (зеленый). Антитела были fm6 (н = 3 на Урбани; н = 5 для SHC014-МА15)11,12 (а), 230.15 (н = 3 на Урбани; н = 2 для SHC014-МА15) (б), 227.15 (н = 3 на Урбани; н = 5 для SHC014-МА15) (С) а 109.8 (н = 3 на Урбани; н = 2 для SHC014-МА15)13 (Д). Каждая точка данных представляет собой групповое среднее значение, а полосы ошибок определяют s.e.m. Обратите внимание, что полосы ошибок в зараженных SARS-CoV Urbani клетках Vero в b,c перекрываются символами и не видны.
Чтобы оценить эффективность существующих вакцин против инфекции SHC014-MA15, мы вакцинировали пожилых мышей дважды инактивированным цельным SARS-CoV (DIV). Предыдущая работа показала, что DIV может нейтрализовать и защитить молодых мышей от заражения гомологичным вирусом; однако вакцина не смогла защитить пожилых животных, у которых также наблюдалась усиленная иммунная патология, что указывало на возможность нанесения вреда животным из-за вакцинации. Здесь мы обнаружили,что DIV не обеспечивает защиту от заражения SHC014-MA15 в отношении потери веса или вирусного титра (дополнительный рис . 5а, б). В соответствии с предыдущим сообщением с другими гетерологичными группами 2b CoV, сыворотка от DIV-вакцинированных пожилых мышей также не смогла нейтрализовать SHC014-MA15 (дополнительный рис. 5c).
В частности, вакцинация DIV привела к стойкой иммунной патологии (Дополнительная таблица 4) и эозинофилии (Дополнительный рис. 5d–f). В совокупности эти результаты подтверждают, что вакцина DIV не будет защищать от инфекции SHC014 и, возможно, может усилить заболевание в возрастной вакцинированной группе.
В отличие от вакцинации мышей с DIV, использование SHC014-MA15 в качестве живой, аттенуированной вакцины показало потенциальную перекрестную защиту против атипичной пневмонии, но результаты имеют важные предостережения. Мы заразили молодых мышей 104 p.f.u. SHC014-MA15 и наблюдал их в течение 28 дней. Затем мы заразили мышей SARS-MA15 на 29-й день (дополнительный рис. 6а). Предшествующее заражение мышей высокой дозой SHC014-MA15 обеспечивало защиту от вызова летальной дозой SARS-MA15, хотя была только минимальная реакция нейтрализации SARS-CoV со стороны антисыворотки, вызванной через 28 дней после заражения SHC014-MA15 (рис. 6б, 1:200). При отсутствии вторичного антигенового усиления 28 d.p. i. представляют собой ожидаемый пик титров антител и подразумевают, что со временем защита от АТИПИЧНОЙ пневмонии будет снижена. Аналогичные результаты,свидетельствующие о защите от заражения летальной дозой SARS-CoV, наблюдались у пожилых мышей BALB/c в отношении потери веса и репликации вируса (Дополнительный рис. 6с, г). Однако инфекционная доза SHC014-MA15 составляет 104 p.f.u. индуцировала потерю веса на более 10% и летальность у некоторых пожилых животных (рис. 1 и дополнительный рис. 3). Мы обнаружили, что вакцинация более низкой дозой SHC014-MA15 (100 p.f.u.) не вызывала потери веса, но и не защищала пожилых животных от смертельной дозы SARS-MA15 (Дополнительный рис. 6e,f). Вместе взятые данные свидетельствуют о том, что заражение SHC014-MA15 может обеспечить перекрестную защиту от SARS-CoV через сохраненные эпитопы, но требуемая доза индуцирует патогенез и исключает использование в качестве аттенуированной вакцины.
Установив, что спайк SHC014 обладает способностью опосредовать инфекцию клеток человека и вызывать заболевание у мышей, мы затем синтезировали полноразмерный инфекционный клон SHC014-CoV на основе подхода, используемого для SARS-CoV (рис. 3а). Репликация в клетках Vero не выявила дефицита SHC014-CoV по сравнению с таковым для SARS-CoV (рис. 3б), однако SHC014-CoV был значительно ослаблен в первичных культурах HAE как через 24, так и через 48 часов после заражения (рис. 3c). Инфекция мышей in vivo не продемонстрировало значительной потери веса, но показало снижение репликации вируса в легких при полноразмерной инфекции SHC014-CoV по сравнению с SARS-CoV Urbani (рис. 3d,е). В совокупности результаты устанавливают жизнеспособность полноразмерного SHC014-CoV, но предполагают, что требуется дальнейшая адаптация для того, чтобы его репликация была эквивалентна репликации эпидемического SARS-CoV в респираторных клетках человека и мышей.
Рис. 3: Полноразмерный SHC014-CoV реплицируется в дыхательных путях человека, но не обладает вирулентностью эпидемического SARS-CoV.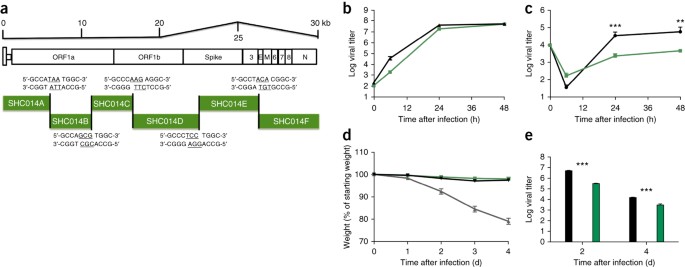
(а) схематическое изображение SHC014-CoV молекулярного клона, который был синтезирован в виде шести непрерывных кДНК (обозначенных SHC014A, SHC014B, SHC014C, SHC014D, SHC014E и SHC014F) в окружении уникальных BglI-сайтов, которые допускаю возможность для направленной сборки полноразмерных кДНК, экспрессирующих открытые рамки считывания (для 1а, 1б, Спайк, 3, конверт, матрица, 6-8 и нуклеокапсиды). Подчеркнутые нуклеотиды представляют собой выступающие последовательности, образующиеся после расщепления фермента рестрикции. (b,c) Вирусная репликация SARS-CoV Urbani (черным) или SHC014-CoV (зеленым) после инфицирования клеток Vero (b) или хорошо дифференцированные, первичные воздушно-жидкостные интерфейсные культуры клеток HAE (c) при MOI 0,01. Образцы отбирали в отдельные моменты времени с биологическими репликами (n = 3) для каждой группы. Данные представляют собой один эксперимент для клеток Vero и HAE. (d,e) Потеря веса (н = 3 для SARS-CoV МА15, н = 7 для SHC014-CoV; П = 6 для SARS-Урбани) (д) и вирусной репликации в легких (П = 3 для SARS-Урбани и SHC014-CoV) (е) от 10-недельных мышей линии balb/с, инфицированных 1 × 105 p.f.u. SARS-CoV MA15 (серый), SHC014-CoV (зеленый) или SARS-CoV Urbani (черный) по i.n. маршруту. Каждая точка данных представляет собой среднее значение группы, а полосы ошибок определяют s.e.m. **P < 0,01 и ***P < 0,001 с использованием t-критерия двухвостого Стьуденческого т-теста для отдельных временных точек.
Во время эпидемии SARS-CoV были быстро установлены связи между пальмовыми циветтами и штаммами CoV , которые были обнаружены у людей.
Основываясь на этом открытии, общая парадигма возникновения утверждает, что эпидемический SARS-CoV возник как вирус летучей мыши, перескочивший на циветт и внесший изменения в рецептор-связывающий домен (RBD) для улучшения связывания циветт с Ace2 (ref. 18).
Последующее воздействие на людей на рынках живых животных позволило заразить человека штаммом циветты, который, в свою очередь, адаптировался к эпидемическому штамму (рис. 4а).
Однако филогенетический анализ показывает, что ранние штаммы SARS человека, по-видимому, более тесно связаны со штаммами летучих мышей, чем со штаммами циветт.
Таким образом, вторая парадигма утверждает, что прямая передача инфекции от летучих мышей человеку инициировала возникновение SARS-CoV и что ладониевые циветты послужили вторичным хозяиноми резервуаром для продолжения инфекции (рис. 4б). Для обеих парадигм адаптация спайка во вторичном хозяине рассматривается как необходимость, причем большинство мутаций, как ожидается, произойдет в пределах RBD, тем самым способствуя улучшению инфекции. Обе теории предполагают, что пулы CoV летучих мышей ограничены и что мутации в диапазоне хозяина являются как случайными, так и редкими, что снижает вероятность будущих событий появления у людей.
Последний раз редактировалось: dimslav (Ср Июн 23, 2021 4:10 pm), всего редактировалось 1 раз(а) (Обоснование : редакция дмитрия)
dimslav- Сообщения : 15403
Дата регистрации : 2017-04-29
Возраст : 55
 Re: Ученые и журналисты: США заранее готовились к COVID-19
Re: Ученые и журналисты: США заранее готовились к COVID-19
- 2б:
Рисунок 4: Парадигмы возникновения коронавирусов.
Штаммы коронавируса сохраняются в квазивидовых пулах, циркулирующих в популяциях летучих мышей. (а,б)
Традиционные теории возникновения SARS-CoV утверждают, что мутанты диапазона хозяина (красный круг) представляют случайные и редкие случаи, которые позволяют заражать альтернативных хозяев. Парадигма вторичного хозяина (а) утверждает, что нечеловеческий хозяин заражен вирусом-прародителем летучих мышей и через адаптацию облегчает передачу людям; последующая репликация у людей приводит к эпидемическому вирусному штамму. Прямая парадигма (b) предполагает, что передача происходит между летучими мышами и людьми без необходимости промежуточного хозяина; отбор затем происходит в человеческой популяции с близкородственными вирусами, реплицирующимися во вторичном хозяине, что позволяет продолжать вирусную устойчивость и адаптацию у обоих. (с) Данные химерных вирусов, подобных SARS, доказывают, что пулы квазивидов содержат множество вирусов, способных заражать человеческие клетки без необходимости мутаций (красные круги). Хотя для возникновения эпидемии может потребоваться адаптация у вторичных или человеческих хозяев, если вирусы, содержащие шипы SHC014, рекомбинируются с вирулентными основами CoV (круги с зелеными контурами), то эпидемическое заболевание может быть результатом у людей. Существующие данные поддерживают элементы всех трех парадигм.
Хотя наше исследование не опровергает другие пути возникновения, оно доказывает существование третьей парадигмы, в которой циркулирующие пулы мышей с CoV поддерживают "уравновешенные" спайковые белки, способные заражать людей без мутаций или адаптации (рис. 4с). Эта гипотеза иллюстрируется способностью химерного вируса, содержащего спайк SHC014 в основе SARS-CoV, вызывать устойчивую инфекцию как в культурах дыхательных путей человека, так и у мышей без адаптации к RBD.
В сочетании с наблюдением ранее выявленных патогенных CoV наши результаты свидетельствуют о том, что исходные материалы, необходимые для возникновения SARS подобных штаммов, в настоящее время циркулируют в резервуарах для животных. Примечательно, что хотя полноразмерный SHC014-CoV, вероятно, требует дополнительной адаптации основы для опосредованного заболевания человека, документированные высокочастотные события рекомбинации в семействах CoV подчеркивают возможность будущего возникновения и необходимость дальнейшей подготовки.
На сегодняшний день геномные экраны популяций животных в основном используются для выявления новых вирусов в условиях вспышек. Подход здесь расширяет эти наборы данных для изучения вопросов возникновения вирусов и терапевтической эффективности. Мы рассматриваем вирусы со спайком SHC014 как потенциальную угрозу из-за их способности размножаться в первичных культурах дыхательных путей человека - наилучшей доступной модели заболевания человека. Кроме того, наблюдаемый патогенез у мышей указывает на способность SHC014-содержащих вирусов вызывать заболевания в моделях млекопитающих без адаптации к RBD.
Примечательно, что дифференциальный тропизм в легких по сравнению с таковым при SARS-MA15 и ослабление полноразмерного SHC014-CoV в культурах HAE по отношению к SARS-CoV Urbani предполагают, что факторы, выходящие за пределы связывания ACE2,-в том числе спайковая процессивность, био—доступность рецепторов или антагонизм иммунных реакций хозяина-могут способствовать возникновению. Однако необходимы дальнейшие исследования на нечеловеческих приматах, чтобы перевести эти результаты в патогенный потенциал человека.
Важно отметить, что отсутствие доступных терапевтических средств определяет критическую потребность в дальнейших исследованиях и разработке методов лечения. С помощью этих знаний могут быть разработаны программы наблюдения, диагностические реагенты и эффективные методы лечения, которые защищают от появления специфических ковидов группы 2b, таких как SHC014, и они могут быть применены к другим ветвям ковидов, которые поддерживают аналогичные гетерогенные пулы.
В дополнение к предложению подготовки против будущих появляющихся вирусов этот подход должен рассматриваться в контексте санкционированной правительством США паузы в исследованиях усиления функции (GOF).
Исходя из предыдущих моделей возникновения (рис. 4а,б), создание химерных вирусов типа SHC014-MA15 не предполагало повышения патогенности. Хотя SHC014-MA15 ослаблен по отношению к своему родительскому адаптированному к мышам SARS-CoV, аналогичные исследования, изучающие патогенность COV с шипом Urbani дикого типа в магистрали MA15, не показали снижения веса у мышей и снижения вирусной репликации. Таким образом, по сравнению с Urbani спайк–MA15 CoV SHC014-MA15 снова проявляется в патогенезе (рис. 1).
На основании этих выводов группы научных обзоров можно посчитать подобные исследования по созданию химерных вирусов на основе циркулирующих штаммов слишком рискованными, поскольку нельзя исключать повышенную патогенность в моделях млекопитающих.
В сочетании с ограничениями на адаптированные к мышам штаммы и разработкой моноклональных антител с использованием беглецов-мутантов исследования возникновения КоВ и терапевтической эффективности могут быть серьезно ограничены в будущем. В совокупности эти данные и ограничения представляют собой перекресток исследовательских проблем GOF; потенциал подготовки к будущим вспышкам и смягчения их последствий должен быть сопоставлен с риском создания более опасных патогенов. При разработке дальнейшей политики важно учитывать ценность данных, полученных в результате этих исследований, и необходимость дальнейшего изучения этих типов химерных вирусов в сопоставлении с присущими им рисками.
В целом, наш подход использовал данные метагеномики для выявления потенциальной угрозы, исходящей от циркулирующих летучих мышей, подобных SARS CoV SHC014. Из-за способности химерных вирусов SHC014 реплицироваться в культурах дыхательных путей человека, вызывать патогенез in vivo и избегать современной терапии, существует необходимость как наблюдения, так и улучшенной терапии против циркулирующих вирусов, подобных SARS. Наш подход также открывает возможности использования данных метагеномики для прогнозирования появления вирусов и применения этих знаний при подготовке к лечению будущих возникающих вирусных инфекций.Методы
Вирусы, клетки, инфекции in vitro и анализы налета
SARS-CoV Дикого типа (Urbani), адаптированный к мышам SARS-CoV (MA15) и химерный SARS-подобный COV культивировали на клетках Vero E6 (полученных из Медицинского научно-исследовательского института инфекционных заболеваний Армии США), выращенных в модифицированной среде Eagle's Medium (DMEM) Dulbecco (Gibco, CA) и 5% фетальной клоновой сыворотке (FCS) (Hyclone, South Logan, UT) вместе с антибиотиком/антимикотиком (Gibco, Carlsbad, CA). Клетки DBT (Baric laboratory, источник неизвестен), экспрессирующие ортологи ACE2, ранее были описаны как для человека, так и для циветты; последовательность Ace2 летучей мыши была основана на последовательности Rhinolophus leschenaulti, и клетки DBT, экспрессирующие у мышей Ace2, были созданы, как описано ранее.
Эксперименты по псевдотипированию были аналогичны экспериментам с использованием псевдовируса на основе ВИЧ, приготовленного , как описано ранее, и исследованного на клетках HeLa (Уханьский институт вирусологии), которые экспрессировали ортологи ACE2. Клетки HeLa выращивали в минимальной эссенциальной среде (MEM) (Gibco, CA), дополненной 10% FCS (Gibco, CA), как описано ранее.
Кривые роста в Vero E6, DBT, Calu-3 2B4 и первичных эпителиальных клетках дыхательных путей человека были выполнены так, как описано ранее. Ни один из запасов рабочей линии клеток не был аутентифицирован или протестирован на микоплазму в последнее время, хотя исходные запасы семян, используемые для создания рабочих запасов, свободны от загрязнения. Человеческие легкие для культур HAE были закуплены в Университете Северной Каролины в Чапел–Хилле по утвержденным Советом по институциональному обзору протоколам. Культуры HAE представляют собой высокодифференцированный эпителий дыхательных путей человека, содержащий реснитчатые и не реснитчатые эпителиальные клетки, а также бокаловидные клетки. Культуры также выращивают на границе воздух-жидкость в течение нескольких недель перед использованием, как описано ранее.
Вкратце клетки промывали PBS и инокулировали вирусом или муляжом, разведенным в PBS, в течение 40 мин при 37°C. После инокуляции клетки промывали три раза и добавляли свежую среду для обозначения времени "0’. В каждый описанный момент времени было собрано три или более биологических реплик. Ослепление не использовалось ни в одной выборке образцов, и образцы не были рандомизированы. Все культивирование вирусов проводилось в лаборатории уровня биобезопасности (BSL) 3 с резервными вентиляторами в шкафах биобезопасности, как описано ранее нашей группой. Весь персонал носил мощные респираторы для очистки воздуха (Breathe Easy, 3M) с костюмами Tyvek, фартуками и ботинками и был в двойных перчатках.Кластеризация последовательностей и структурное моделирование.
Полноразмерные геномные последовательности и аминокислотные последовательности доменов S1 спайка репрезентативных CoV были загружены из Genbank или Pathosystems Resource Integration Center (PATRIC), выровнены с ClustalX и филогенетически сопоставлены с использованием оценки максимального правдоподобия с использованием 100 бутстрапов или с использованием пакета PhyML соответственно. Дерево было сгенерировано с использованием метода максимального правдоподобия с помощью пакета PhyML. Шкала представляет собой нуклеотидные замены. Помечены только узлы с поддержкой bootstrap выше 70%.
Дерево показывает, что CoV делятся на три различные филогенетические группы, определяемые как α-CoV, β-CoV и γ-CoV. Классические кластеры подгрупп обозначены как 2a, 2b, 2c и 2d для β-CoVs и 1a и 1b для α-CoVs. Структурные модели были сгенерированы с помощью Modeller (Max Planck Institute Bioinformatics Toolkit) для генерации гомологических моделей SHC014 и Rs3367 SARS RBD в комплексе с ACE2 на основе кристаллической структуры 2AJF (Protein Data Bank). Модели гомологии были визуализированы и обработаны в MacPyMol (версия 1.3).Конструирование химерных вирусов, подобных SARS.
Как дикие, так и химерные вирусы были получены либо из SARS-CoV Urbani, либо из соответствующего адаптированного к мышам (SARS-CoV MA15) инфекционного клона (ic), как описано ранее.
Плазмиды, содержащие спайковые последовательности для SHC014, экстрагировали рестрикционным дайджестом и лигировали в плазмиду E и F инфекционного клона MA15. Клон был разработан и приобретен у Bio Basic в виде шести смежных кДНК с использованием опубликованных последовательностей, фланкированных уникальными сайтами эндонуклеазы рестрикции II класса (BglI). После этого плазмиды, содержащие фрагменты генома дикого типа, химерные SARS-CoV и SHC014-CoV, были амплифицированы, вырезаны, лигированы и очищены.
Затем были проведены транскрипционные реакции In vitro для синтеза полноразмерной геномной РНК, которая была трансфицирована в клетки Vero E6, как описано ранее. Среда из трансфицированных клеток собиралась и служила семенным материалом для последующих экспериментов. Химерные и полноразмерные вирусы были подтверждены анализом последовательностей перед использованием в этих исследованиях. Синтетическая конструкция химерного мутанта и полноразмерного SHC014-CoV была одобрена Институциональным комитетом по биобезопасности Университета Северной Каролины и комитетом по исследованиям двойного назначения концерна.Этическое заявление
Это исследование было проведено в соответствии с рекомендациями по уходу и использованию животных Управления по охране лабораторных животных (OLAW), NIH. Институциональный комитет по уходу и использованию животных (IACUC) Университета Северной Каролины в Чапел-Хилле (UNC, Разрешение № A-3410-01) одобрил протокол исследования животных (IACUC № 13-033), используемый в этих исследованиях.Мыши и инфекция in vivo
Самки, 10-недельные и 12-месячные мыши BALB/cAnNHsD были заказаны в Harlan Laboratories. Заражение мышей проводилось так, как было описано ранее. Вкратце, животных приводили в лабораторию BSL3 и позволяли акклиматизироваться в течение 1-й недели до заражения. Для заражения и вакцинации живым ослабленным вирусом мышей анестезировали смесью кетамина и ксилазина и заражали интраназально, когда им вводили 50 мкл фосфатно-буферного физиологического раствора (PBS) или разбавленного вируса тремя или четырьмя мышами в каждый момент времени, на каждую инфекционную группу в дозе, как описано в легендах рисунка.
Для отдельных мышей обозначения инфекции, включая неспособность вдохнуть всю дозу, пузырение инокулята из носа или инфекцию через рот, могли привести к исключению данных по мышам по усмотрению исследователя; после заражения никакие другие заранее установленные критерии исключения или включения не определены. Ослепление не применялось ни в одном эксперименте на животных, и животные не были рандомизированы. Для вакцинации молодых и старых мышей вакцинировали инъекцией подушечки ноги объемом 20 мкл либо 0,2 мкг двойной инактивированной вакцины SARS-CoV с квасцами, либо имитацией PBS; затем мышам вводили повторную вакцинацию по той же схеме через 22 дня, и заражали через 21 день.
Во всех группах, согласно протоколу, животных ежедневно наблюдали за наличией клинических признаков заболевания (сгорбленность, взъерошенная шерсть, снижение активности) в течение всего эксперимента. Потеря веса контролировалась ежедневно в течение первых 7 дней, после чего контроль веса продолжался до тех пор, пока животные не восстановились до своего первоначального исходного веса или не показали непрерывную прибавку веса в течение 3 дней.
Всех мышей, потерявших более 20% от исходной массы тела, кормили наземным кормом и дополнительно контролировали несколько раз в день, пока они находились под 20%-ным ограничением. Мышей, потерявших более 30% от исходной массы тела, немедленно умерщвлялась в соответствии с протоколом. Любая мышь, считавшаяся умирающей или вряд ли выздоровевшей, также гуманно умерщвлялась по усмотрению исследователя. Эвтаназия была проведена с использованием передозировки изофлурана, и смерть была подтверждена вывихом шейки матки. Все исследования на мышах проводились в Университете Северной Каролины (Animal Welfare Assurance #A3410-01) с использованием протоколов, одобренных Комитетом UNC Institutional Animal Care and Use Committee (IACUC).Гистологический анализ.
Левое легкое удаляли и погружали в 10%-ный буферный формалин (Фишер) без надувания в течение 1-й недели. Ткани погружали в парафин, а срезы размером 5 мкм готовили в центре гистопатологии Комплексного онкологического центра UNC Lineberger. Чтобы определить степень окрашивания антигеном, срезы окрашивали на вирусный антиген с использованием коммерчески доступного поликлонального антинуклеокапсидного антитела SARS-CoV (Imgenex) и оценивали слепым способом путем окрашивания дыхательных путей и паренхимы, как описано ранее. Изображения были получены с помощью микроскопа Olympus BX41 с камерой Olympus DP71.Анализы нейтрализации вирусов.
Анализ титра нейтрализации уменьшения налета проводили с использованием ранее охарактеризованных антител против SARS-CoV, как описано ранее,
12,13
Вкратце, нейтрализующие антитела или сыворотку последовательно разбавляли в два раза и инкубировали со 100 ед. различных инфекционных клонов штаммов SARS-CoV в течение 1 ч при 37 °C. Затем вирус и антитела добавляли к 6-луночной пластине с 5 × 105 клетками Vero E6/лунка с множественными репликами (n ≥ 2). После 1-часовой инкубации при 37 °С клетки накладывали на среду 3 мл 0,8% агарозы. Пластины инкубировали в течение 2 дней при 37 °С, окрашивали нейтральным красным в течение 3 ч и подсчитывали налеты. Процент уменьшения налета рассчитывали как (1 − (количество налета с антителом/количество налета без антитела)) × 100.Статистический анализ
Все эксперименты проводились в двух экспериментальных группах (либо два вируса, либо вакцинированная и невакцинированная когорты). Таким образом, достоверные различия в титре вируса и оценке гистологии определялись с помощью двухвостого Студенческого т-теста в отдельные моменты времени. Данные были нормально распределены в каждой сравниваемой группе и имели одинаковую дисперсию.Биобезопасность и биозащита
Отчетные исследования были начаты после того, как Институциональный комитет по биобезопасности Университета Северной Каролины одобрил экспериментальный протокол (Название проекта: Генерация инфекционных клонов летучих мышей SARS-like CoV; Lab Safety Plan ID: 20145741; Schedule G ID: 12279).
Эти исследования были начаты до того, как правительство США приостановило финансирование отдельных исследований, связанных с повышением функций, включая вирусы гриппа, MERS и SARS. Этот документ был рассмотрен финансовым агентством минздрава NIH. Было предложено продолжить эти исследования, и это было одобрено NIH.
SARS-CoV - это особый агент. Все работы по этим исследованиям проводились в соответствии с утвержденными стандартными рабочими процедурами (СОП) и условиями безопасности для SARS-CoV, MER-CoV и других связанных CoV. Наши институциональные объекты CoV BSL3 были разработаны в соответствии с требованиями безопасности, которые рекомендуются в области биобезопасности в микробиологических и биомедицинских лабораториях (BMBL), Министерстве здравоохранения и социальных служб США, Службе общественного здравоохранения, Центрах по контролю заболеваний (ЦКЗ) и минздраве. Планы безопасности лаборатории были представлены, и объект был одобрен для использования Департаментом охраны окружающей среды и безопасности окружающей среды ООН (EHS) и ЦКЗ. Для входа в заведение требуется электронная карта доступа.
Все работники были обучены служащими EHS безопасному использованию мощных респираторов для очистки воздуха (PAPR), а также соответствующим рабочим навыкам в работе с BSL3, выполняются планы активного медицинского наблюдения. Наши объекты CoV BSL3 содержат резервные вентиляторы, аварийное питание вентиляторов и шкафы биологической безопасности и морозильные камеры, а также наши объекты могут вместить стеллажи для мышей SealSafe. Материалы, классифицированные как агенты BSL3, состоят из штаммов-предшественников SARS-CoV, bat-CoV, MERS-CoV и мутантов, полученных из этих патогенов. В установках BSL3 эксперименты с инфекционным вирусом проводятся в сертифицированном Кабинете биобезопасности класса II (BSC).
Все сотрудники носят халаты, костюмы и фартуки "Тайвек", папры и бахилы, а на руках - двойные перчатки. Пользователи BSL3 подпадают под действие плана медицинского наблюдения, контролируемого Университетской клиникой профессионального здоровья сотрудников (UEOHC), который включает ежегодное физическое обследование, ежегодную вакцинацию против гриппа и обязательное сообщение о любых симптомах, связанных с CoV-инфекцией в периоды работы в BSL3. Все пользователи BSL3 обучены управлению экспозицией и протоколам отчетности, подготовлены к самокарантину и прошли обучение безопасной доставке в местный отдел управления инфекционными заболеваниями в чрезвычайной ситуации. Все потенциальные события воздействия сообщаются и исследуются EHS и UEOHC, а отчеты направляются как в ЦКЗ, так и в минздрав.Коды присоединения
Присоединение
Банк данных белков
- 2AJF
История изменений
20 Ноября 2015 года
В версии этой статьи, первоначально опубликованной в Интернете, авторы не признали источник финансирования, USAID-EPT-PREDICT funding from EcoHealth Alliance, до Z.-L. S. Ошибка была исправлена для печатных, PDF и HTML версий этой статьи.- 2AJF
Последний раз редактировалось: dimslav (Чт Июн 24, 2021 8:45 am), всего редактировалось 2 раз(а) (Обоснование : редакция дмитрия)
dimslav- Сообщения : 15403
Дата регистрации : 2017-04-29
Возраст : 55
 Похожие темы
Похожие темы» Карен Кингстон - Развенчание обмана COVID-19: "Роман" коронавируса
» Правда.ру - Ученые и журналисты: США заранее готовились к COVID-19Коронавирус COVID-19: случайность или биооружие?
» Главные причины, почему многие люди, врачи и учёные отказываются ставить вакцину от COVID
» Карен Кингстон-у Джима Фергюсона-турбо-раки находятся в патентах, это было заранее спланировано
» Сергей Мальцев - Краткий путеводитель по covid-вакцинации. + Covid-викторина! вопросы знатокам и другие статьи
» Правда.ру - Ученые и журналисты: США заранее готовились к COVID-19Коронавирус COVID-19: случайность или биооружие?
» Главные причины, почему многие люди, врачи и учёные отказываются ставить вакцину от COVID
» Карен Кингстон-у Джима Фергюсона-турбо-раки находятся в патентах, это было заранее спланировано
» Сергей Мальцев - Краткий путеводитель по covid-вакцинации. + Covid-викторина! вопросы знатокам и другие статьи
Школа Души Божественного Космоса :: В поисках правды: инсайдеры и теории заговоров :: Разоблачители коронамракобесия
Страница 1 из 1
Права доступа к этому форуму:
Вы не можете отвечать на сообщенияПоднимись к оглавлению форума




» Ана Михалча Трансгуманистическая технократия продолжается беседа с Питером Кенигом
» На чём основана ваша любовь к Путину
» Дэвид Айк Освобожденный трансгуманизм_
» Джин Декоуд #46 Землетрясения уничтожают DUMBS в SaltLake, Австралии, Африке, Азии плюс вакцина-убийца 2015
» ИЗАБЕЛЛА А. ГРИН - ПО ТУ СТОРОНУ ЛОВУШКИ Скрытая правда о Реинкарнации (книга 2)
» Интервью 5 Джин Декоуд
» Это Великая война Добра и Зла
» Брэдли Любящий Правда об истине
» Гидеон - Разведданные № 53 — победа Трампа и грядущий крах финансовой системы
» Роберт Дункан Одно из последних интервью
» Брэдли ПОДКАСТ 131 КОТОРЫЙ СОЕДИНЯЕТ ВСЕ, ЧТО ВАМ НУЖНО ЗНАТЬ, ВМЕСТЕ
» Вот почему вы БОИТЕСЬ правды
» Брэдли Любящий PODCAST N°132 - КОГДА ВЫ НАХОДИТЕСЬ В ПРОСТРАНСТВЕ ГОСПОДНЕМ, ВЫ НАХОДИТЕСЬ И В ПРОСТРАНСТВЕ ИСТИНЫ И ВЕЧНОЙ ЖИЗНИ
» ДР. ДЖЕЙН РУБИ - Обман повсюду, даже от людей, которым вы доверяете
» Инфляция как результат высокой ставки - Трамп, Хазин и др.
» Наша новая реальность Карен Хьюдс
» Алан Уотт Авторы Эпизод 16 Кэрролл Куигли Формирование империи Ноябрь 9, 2024
» Эбен Александер - Смерть организма и мозга, не означает смерть сознания +Параллельные миры Эбена Александера.
» Победитель 7 сезона рассказал всю правду о "Битве экстрасенсов"
» Михаил Кузнецов - Зачем нам показали планету Нибиру?
» Ашаяна Дин - Наследие Лемурии и Атлантиды. Семинар на 11 часов, три дня на 5 дисках
» Дэвид_Айк_Результаты_выборов_в_США_что_это_значит
» Саша Латыпова Анафилаксия от вакцин - обсуждение с доктором Джейн Руби
» Доктор Майк Йидон раскрывает тему травм, полученных при применении ваксы - Вена, Австрия
» Тайные люди_ Кэрролл Куигли
» Ана Михалча Электронно-полевая микроскопия пробирок ковид19 и живой крови - Беседа доктора Хортеники Бремер
» Видео. ИЗАБЕЛЛА А. ГРИН - «Темная ловушка души смерти! Завершение цикла реинкарнации» [Age Of Truth TV]
» ИЗАБЕЛЛА А. ГРИН - ПОКИДАЯ ЛОВУШКУ Как выйти из цикла Реинкарнации. Кн.1
» Фтористый яд в кране
» Брэдли Любящий ЭТО НЕ ИГРА
» Бенджамин Фулфорд: еженедельный отчет за 11.11.2024
» Давайте посмотрим, как удалить оксид графена только с помощью Oration
» 2024-10-24_Карен Кингстон- Maria Zeee
» Кэти О'Брайен обсуждает сатанинский Контроль над Разумом с Николасом Вениамином
» К Кингстон у Эмеральды 1 ноября 2024
» Филадельфийский эксперимент и Монтокский проект-
» Квантовая Реальность и Пробуждение Сознания – Эксклюзив с Дэвидом Айком
» Служба защиты детей - преступная организация Дэвид Стрейт
» Ашаяна Дин о неестественном выходе из цикла смерти,как выглядит активация ДНК в 3Д мире. Часть лекции на три часа
» Курт Р. Калленбах Свидетельство о рождении
» Брэдли Любящий КТО НА САМОМ ДЕЛЕ РАЗРУШАЕТ ЗЕМЛЮ И — «О, КАКУЮ ЗАПУТАННУЮ СЕТЬ МЫ ПЛЕТЕМ…»
» Книжный уголок "У Шизотерика" - новые книги по эзотерике и не только...
» КЕРРИ КЭССИДИ ТАЙНОЕ КОСМИЧЕСКОЕ РАСКРЫТИЕ РОУЗВЕЛЛА И ПРОЕКТ «ГОЛУБОЙ ЛУЧ»
» КЕРРИ КЭССИДИ ПОЧЕМУ ПОБЕДИЛ ТРАМП: ИЛЛЮМИНАТЫ СМЕНИЛИ СТОРОНУ
» Ким гоген Перемены начинаются с тебя
» ШЕРРИ ТЕНПЕННИ ОБЪЯСНЯЕТ, КАК ДЕПОПУЛЯЦИОННЫЕ ВАКЦИНЫ КОВИД НАЧНУТ ДЕЙСТВОВАТЬ ЧЕРЕЗ 3-6 МЕСЯЦЕВ
» Ким Гоген - Настоящая история Земли
» Карен Кингстон — предупреждение о новой пандемии, убийственных вакцинах и намеренном уничтожении продовольствия
» Что такое «Флибуста»
» Тьерри Мейсан Место США и Израиля в правительствах ЕС и Франции
» Тьерри Мейсан НАТО, мигранты в ЕС и надвигающаяся война в Приднестровье
» XVI Саммит БРИКС: Казанская декларация
» Тьерри Мейсан Саммит в Казани перевернул мир с головы на ноги
» Тьерри Мейсан За взаимными обвинениями Израиля и Ирана кроется реорганизация ближневосточных альянсов
» Тьерри Мейсан Иран и Израиль
» Время перемен (...снова) - Дэвид Айк.
» Лара Логан и Саша Латыпова о сокрытии VAXX в минобороны с FDA
» Надвигающийся финансовый крах - Дэвид Айк
» Быстрые огненные ответы на вопросы Дэвида Айка в 2020 году
» Марк Пассио - 10_24_2024 Повестка дня 2030 Аарон Дэй Шоу Майкл
» Разговор суперсолдата - Джимми Пейн - Звездный путь Энтерпрайз
» Бенджамин Фулфорд: еженедельный отчет за 4 ноября 2024
» Новое правило_ Вместе с гордостью _ Реальное время с Биллом Махером
» Unrestricted Warfare Ep. 186 Трансчеловеческая антиутопия с доктором Аной Михалчей, доктором Джо Сансоне
» Карен Дэнрич «Мила» - История человечества. Фальшивые Вознесенные Мастера
» Смерть. Стадии умирания, смерти и постсмертии.
» Бенджамин Фулфорд и Джим-Уилли - самое большое раскрытие, которого никто не ожидал
» Михаил Кузнецов - Что является главной движущей силой "борьбы с лженаукой" - тупость или продажность наемных болтунов?
» Документальный фильм, который потряс Грецию - SKAI 1821
» Уэс Пенре - Битвы между тенью и светом (новая книга 2024 года)
» Беседа с Джейми Эндрюсом, проект Virology Controls Studies.Саша Латыпова
» Марк Пассио - Священный дар гнева (полная лекция)
» ДР. ДЖЕЙН РУБИН - ОБРАЩЕНИЕ БОЛЕЗНЕЙ ВСПЯТЬ С ПОМОЩЬЮ КВАНТОВОГО ЗДОРОВЬЯ II
» Внутренняя алхимия для женщин - РОБЕРТ СЕПЕР
» Министерство обороны, правительство США, Большая Фарма - все это одно целое - доктор Джейн Руби беседует с Гаретом Айком.rus
» Питер Мейер - Как спастись от своего рабства 2024/10/28
» Питер Мейер - Раскрытие приносит свет 2024/10/24/
» Питер Мейер - Знания ведут к здоровому образу жизни и свободе 2024/10/21/
» Надвигающийся закон военного времени предупреждает_ Доктор Наоми Вульф предупреждает, что Америка в состоянии войны с глобалистамм
» Беседа суперсолдата - Исмаэль Перес - Наше космическое происхождение.rus
» Ложная тревога по поводу климата - Дэвид Айк
» Парижская Олимпиада_ Когда колдовство не удается.рус
» Бенджамин Фулфорд: еженедельный отчет от 28.10.2024
» серия фильмов Vaxxed 1-3 с переводом
» Брэдли Любящий PODCAST N° 130 - ПРЕОДОЛЕВАЕМ СОВРЕМЕННЫЕ ТЕХНОЛОГИИ ОРУЖИЯ, НАПРАВЛЕННЫЕ НА ВАШЕ МЫШЛЕНИЕ, ТЕЛО И ДУШУ
» Михаил Кузнецов - Дэвид Айк о Лунной Матрице
» Михаил Кузнецов - Пророчества одесского старца о судьбе Украины.
» Михаил Кузнецов - Свидетельство антарктического пилота. Синий лед из-за купола + Сноуден подтвердил теорию "полой Земли" + Американский ученый об артефактах Антарктиды
» М. Кузнецов - Как работает намерение. Джо Диспенза. Как выстраивать новое возможное будущее?
» М. Кузнецов - Цикл статей о Колесах времени
» Михаил Кузнецов - Путешествия в нашем мире с помощью техники сновидения. В 3 частях Фиксация точки сборки и др. статьи об ОС
» Брэдли Любящий Хаос и неразбериха — последние ингредиенты, необходимые для разрушения цивилизации. Часть первая
» ДЖОН ЛЭМБ ЛЭШ - ИИ против ненависти ~ Иллюзия сострадания - изменение игры
» БЕНДЖАМИН ФУЛФОРД И КИМ ГОГЕН 9 марта 2022
» МЕДИЦИНСКАЯ ТИРАНИЯ БОМБШЕЛЛ_ Инсайдер индустрии Бриам Бюлер раскрывает секреты Большой Фармы
» 2024-08-27_проект_веритас о прививках
» ГИДЕОН - Бюллетень Разведданных - планы Обсидиана на 2025 год, USDR, утечка данных и многое другое
» Доктор Кэрри Мадей Вакцины против столбняка используются для контроля рождаемости Депопуляция человечества